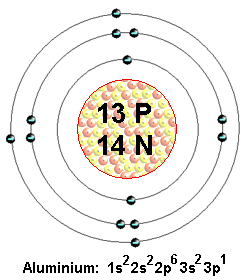
alumínio-27 é um isótopo de alumínio caracterizado pelo fato de que tem um número de massa igual a #27#.
Agora, o número de massa de um átomo diz-lhe o número total de protões e de neutrões que o átomo tem no seu núcleo. Uma vez que está a lidar com um isótopo de alumínio, segue-se que este átomo deve ter exactamente o mesmo número de protões no seu núcleo.
O número de prótons que um átomo tem no seu núcleo é dado pelo número atómico., Um olhar rápido na tabela periódica irá mostrar que o alumínio tem um número atômico igual a # 13#. isto significa que qualquer átomo que seja um isótopo de alumínio terá prótons # 13# no seu núcleo. uma vez que está a lidar com um átomo neutro, o número de electrões que rodeiam o núcleo deve ser igual ao número de protões encontrados no núcleo.
portanto, o isótopo alumínio-27 terá #13# elétrons em torno de seu núcleo.,
finalmente, use o número de massa conhecido para determinar quantos neutrões você tem
#cor(Azul)(“número de massa” = “no. of protons ” + ” no. of neutrons”)#
# ” no. de nêutrons” = 27 – 13 = 14#