data di pubblicazione: 22 dicembre 2014
Trans-Tasman Sistema di allerta Precoce – Avviso di Comunicazione
Domperidone (Motilium Prokinex) – conclusione di una revisione dei benefici e dei rischi di danno
i Prodotti affetti
Informazioni per i consumatori e assistenti
Informazioni per i professionisti sanitari,
controllare il Riepilogo
Quali sono le azioni Medsafe prendendo?
Come segnalare eventi avversi
Ulteriori informazioni
Domperidone è un farmaco anti-nausea che ha proprietà gastroprokinetiche., Domperidone è usato per trattare:
- sintomi dispeptici che possono essere associati a svuotamento gastrico ritardato (ad esempio, senso di pienezza epigastrico, distensione o gonfiore addominale, dolore o disagio epigastrico) e
- sintomi acuti di nausea e vomito.
Recenti ricerche hanno suggerito un aumento del rischio di prolungamento del QT (alterazione dell’attività elettrica del cuore), aritmie (battiti cardiaci instabili) e morte cardiaca improvvisa con l’uso di domperidone orale.
Medsafe ha delineato queste preoccupazioni in una comunicazione di monitoraggio pubblicata nel marzo 2014., A causa di queste preoccupazioni, Medsafe e il Medicines Adverse Reactions Committee (MARC) hanno esaminato i benefici e i rischi di danni dei medicinali contenenti domperidone.
Monitoraggio comunicazione: Domperidone (Motilium, Prokinex) ed effetti sul cuore
Medicinali Reazioni avverse Comitato verbale della 158a riunione
Medsafe e il MARC hanno concluso che vi è un piccolo aumento del rischio di effetti cardiaci avversi. Tuttavia, il rapporto tra benefici e rischi potenziali per domperidone rimane favorevole., I dati disponibili suggeriscono che questo piccolo aumento del rischio può essere più elevato nei pazienti di età superiore ai 60 anni o a dosi giornaliere totali superiori a 30 mg.
Nonostante il sostegno delle VINACCE per mantenere una dose massima giornaliera raccomandata di 80 mg, Janssen (produttore del marchio Motilium di domperidone) ha concluso che la dose massima raccomandata deve essere ridotta da 80 mg a 40 mg al giorno. Questa modifica della dose e altre modifiche e aggiunte alle schede tecniche di domperidone sono state raccomandate per gestire i potenziali rischi per il cuore associati all’uso di domperidone.,
i Prodotti affetti
| nome del Prodotto | Sponsor |
|---|---|
| Motilium | Janssen-Cilag (Nuova Zelanda) Ltd |
| Prokinex | Flusso d’Aria Products Limited |
Informazioni per i consumatori e assistenti
- Per la maggior parte delle persone, l’assunzione di domperidone è sicuro. Tuttavia, se ha problemi cardiaci o sta assumendo altri medicinali, deve prima verificare con il medico che questo medicinale sia appropriato.,
- Usi la dose più bassa che funziona per Lei e interrompa appena possibile.
- Se manifesta sintomi come vertigini, svenimenti o palpitazioni cardiache mentre sta assumendo domperidone, deve interrompere l’assunzione di questo medicinale e consultare un medico. Questi sintomi possono essere dovuti ad un ritmo cardiaco anormale causato da domperidone.
- Medsafe non può dare consigli sulle condizioni mediche di un individuo. Se ha dubbi su un medicinale che sta assumendo Medsafe la incoraggia a parlare con il suo operatore sanitario.,
Informazioni per gli operatori sanitari
- Il rapporto beneficio-rischio complessivo di domperidone rimane positivo.
- La dose massima raccomandata di domperidone è stata ridotta da 80 mg al giorno a 40 mg al giorno. Utilizzare la dose efficace più bassa per la durata più breve possibile.
- La dose massima raccomandata nei bambini di peso ≤ 35 kg è di 0,25 mg/kg da tre a quattro volte al giorno fino a 1,0 mg/kg/die. Domperidone è controindicato nei bambini di età inferiore ai 2 anni.,
- Domperidone è stato associato al prolungamento dell’intervallo QT ed è pertanto controindicato con potenti inibitori del CYP3A4 e con altri medicinali che prolungano l’intervallo QTc.
- Domperidone deve essere usato con cautela nei pazienti più anziani o in quelli con malattia cardiaca in corso o anamnesi.
- I pazienti che ricevono una terapia a lungo termine con domperidone devono essere regolarmente esaminati per verificare l’efficacia, gli effetti avversi e lo sviluppo di fattori di rischio cardiovascolare.,
- I fattori di rischio rilevanti per gli eventi cardiovascolari associati a domperidone includono ipertensione, iperlipidemia, obesità, diabete, fumo e consumo eccessivo di alcol.
- Domperidone è indicato per i sintomi dispeptici associati a svuotamento gastrico ritardato e sintomi acuti di nausea e vomito.
- Non vi sono prove sufficienti a sostegno dell’uso di domperidone nella malattia da reflusso gastro-esofageo infantile e potrebbe non essere adatto per nausea e vomito indotti da chemioterapia o radioterapia o nausea e vomito post – operatorio.,
- Altri medicinali usati per trattare i disturbi digestivi o la nausea e il vomito sono stati anche trovati per causare il prolungamento dell’intervallo QTc.
- Discutere i benefici e il rischio di danni del trattamento con domperidone con i pazienti prima di iniziare la terapia. Segnalare eventuali reazioni avverse al Centro di monitoraggio delle reazioni avverse (CARM).
Riassunto della recensione
Il MARC ha esaminato gli ultimi dati nel giugno 2014. Il MARC ha concluso che, mentre l’equilibrio tra benefici e rischio di danni per domperidone rimane favorevole, vi è un piccolo aumento del rischio di effetti cardiaci avversi.,
Molti studi hanno avuto un basso numero di eventi complessivi e i valori di rischio variavano tra i diversi studi. Pertanto, non è stato possibile misurare una stima reale del rischio. Di seguito è riportato un riassunto dei dati esaminati:
Tabella 1: Rischio di morte cardiaca improvvisa: studio caso-controllo basato sulla popolazione1.
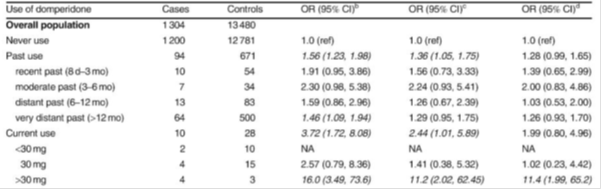
Tabella 2: Rischio di aritmia ventricolare grave e morte cardiaca improvvisa con domperidone in relazione alla mancata esposizione a medicinali in studio o a inibitori della pompa protonica esposizione: studio caso-controllo nidificato basato sulla popolazione2.,
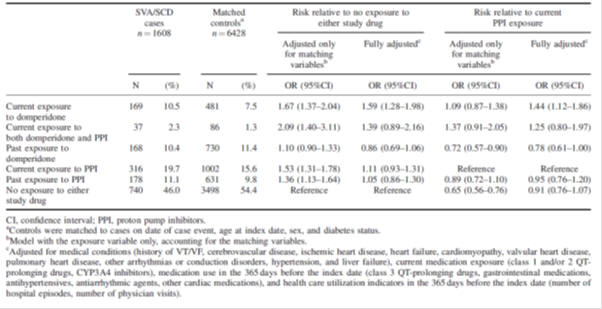
Tabella 3: Valutazione dell’intervallo QTc, prima e durante domperidone amministrazione nei neonati prematuri (n=40)3
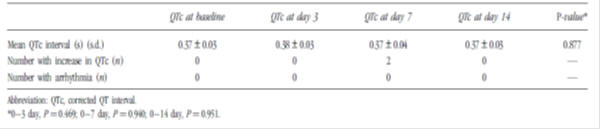
non Ci sono limitazioni per gli studi inclusi nella revisione, come l’osservazione della natura della maggior parte degli studi, una mancanza di informazioni circa l’indicazione per l’uso, la gravità della malattia, il dosaggio e di regime, e di altri fattori di rischio come il fumo di stato, concomitante di farmaci e di co-morbidità. Bias protopatico è quando un trattamento per i primi sintomi di una malattia o altro risultato sembrano causare il risultato., In questa situazione, i pazienti possono essere stati prescritti domperidone per sintomi gastrointestinali non specifici che possono infatti essere i sintomi prodromici della malattia coronarica. Pertanto, il bias protopatico e la confusione per indicazione non possono essere esclusi in molti degli studi osservazionali.
Ulteriori studi esaminati includevano uno studio di sicurezza post-autorizzazione e studi che studiavano gli effetti dell’uso di domperidone sull’intervallo QTc negli adulti., Uno studio approfondito sul QT non ha mostrato alcuna risposta dose-QTc clinicamente rilevante o risposta esposizione-QTc con domperidone; tuttavia i casi di prolungamento del QTc, aritmia e morte cardiaca improvvisa con domperidone significano che questo rischio non può essere completamente escluso.
Il MARC ha osservato che altri tipi di medicinali usati per trattare i disturbi digestivi o la nausea e il vomito sono stati associati anche al prolungamento dell’intervallo QT. Questi fattori devono essere presi in considerazione quando si sceglie la migliore medicina per un singolo paziente.
- van Noord C, Dieleman JP, van Herpen G, et al. (2010)., Domperidone e aritmia ventricolare o morte cardiaca improvvisa: uno studio caso-controllo basato sulla popolazione nei Paesi Bassi. Sicurezza dei farmaci, 33(11): 1003-14
- Johannes CB, Varas-Lorenzo C, McQuay LJ, et al. (2010). Rischio di aritmia ventricolare grave e morte cardiaca improvvisa in una coorte di utenti di domperidone: uno studio caso-controllo nidificato. Pharmacoepidemiology and Drug Safety, 19: 881-88
- Gunlemez A, Babaoglu A, Arisoy AE, et al. (2010). Effetto di domperidone sull’intervallo QTc nei neonati prematuri. Journal of Perinatology, 30: 50-3
Quali azioni stanno prendendo Medsafe?,
Medsafe sta lavorando con gli sponsor di questi prodotti per garantire che le schede tecniche e le informazioni sulla medicina dei consumatori delineino in modo appropriato la sicurezza di domperidone.,ADR app online
Prescrittori possono presentare online utilizzando il tool di reporting a disposizione del paziente, software per la gestione
Medsafe non può dare consigli su di un individuo di una condizione medica., Se ha dubbi su un medicinale che sta assumendo Medsafe la incoraggia a parlare con il suo operatore sanitario.