Publicado em: 22 de dezembro de 2014
Trans-Tasman Sistema de alerta Precoce de Alerta de Comunicação
a Domperidona (Motilium, Prokinex) – conclusão da revisão dos benefícios e riscos de danos
Produtos afetados
Informações para os consumidores e prestadores de cuidados de
Informações para profissionais de saúde
Revisão Resumo
quais as ações Que estão Medsafe tomar?
como notificar acontecimentos adversos
Informação adicional
domperidona é um medicamento anti-náuseas que tem propriedades gastroprocinéticas., Domperidona é utilizado no tratamento de: sintomas dispépticos que podem estar associados ao esvaziamento gástrico retardado (por exemplo, sensação epigástrica de plenitude, distensão ou inchaço abdominal, dor epigástrica ou desconforto) e sintomas agudos de náuseas e vómitos.investigação recente sugeriu um aumento do risco de prolongamento QT (alteração da actividade eléctrica do coração), arritmias (batimentos cardíacos instáveis) e morte cardíaca súbita com o uso de domperidona oral.Medsafe expôs estas preocupações numa comunicação de monitorização publicada em Março de 2014., Devido a estas preocupações, o Medsafe e o Comité de reacções adversas aos medicamentos (MARC) analisaram os benefícios e Riscos dos danos dos medicamentos contendo domperidona.
Acompanhamento de comunicação: Domperidona (Motilium, Prokinex) e efeitos sobre o coração
a Medicamentos as Reações Adversas Comissão de minutos de 158 reunião
Medsafe e o MARC concluíram que há um pequeno aumento do risco de efeitos adversos coração de efeitos. No entanto, o equilíbrio entre os benefícios e os potenciais danos para a domperidona continua a ser favorável., Os dados disponíveis sugerem que este pequeno aumento do risco pode ser maior em doentes com mais de 60 anos de idade ou com doses diárias totais superiores a 30 mg.apesar do apoio do MARC para manter uma dose diária máxima recomendada de 80 mg, Janssen (fabricante da marca Motilium de domperidona) concluiu que a dose máxima recomendada deve ser reduzida de 80 mg para 40 mg por dia. Recomenda-se esta alteração da dose e outras alterações e adições às fichas de dados de domperidona para gerir os potenciais riscos para o coração associados à utilização de domperidona.,
Produtos afetados
| nome do Produto | Patrocinador |
|---|---|
| Motilium | Janssen-Cilag (Nova Zelândia) Ltd |
| Prokinex | Fluxo de Ar Products Limited |
Informações para os consumidores e prestadores de cuidados
- Para a maioria das pessoas, tomando domperidona é seguro. No entanto, se tiver problemas cardíacos ou estiver a tomar outros medicamentos, deve primeiro verificar com o seu profissional de saúde que este medicamento é apropriado.,utilize a dose mais baixa que funciona para si e pare o mais depressa possível.se sentir quaisquer sintomas tais como tonturas, desmaios ou palpitações cardíacas enquanto estiver a tomar domperidona, deve parar de tomar este medicamento e procurar cuidados médicos. Estes sintomas podem ser devidos a um ritmo cardíaco anormal causado pela domperidona. Medsafe não pode dar conselhos sobre a condição médica de um indivíduo. Se tem alguma preocupação com um medicamento que está a tomar Medsafe encoraja-o a falar com o seu profissional de saúde.,
informação para os profissionais de saúde
- a relação benefício-risco global da domperidona permanece positiva.a dose máxima recomendada de domperidona foi reduzida de 80 mg por dia para 40 mg por dia. Utilize a dose eficaz mais baixa durante o menor período possível. a dose máxima recomendada em crianças com peso ≤ 35 kg é de 0, 25 mg/kg três a quatro vezes por dia até 1, 0 mg/kg/dia. Domperidona está contra-indicada em crianças com menos de 2 anos de idade.,a domperidona tem sido associada ao prolongamento do intervalo QT, pelo que está contra-indicada com inibidores potentes do CYP3A4 e com outros medicamentos que prolongam o intervalo QTc. a domperidona deve ser utilizada com precaução em doentes mais velhos ou com doença cardíaca actual ou histórica. os doentes em tratamento prolongado com domperidona devem ser regularmente avaliados quanto à eficácia, efeitos adversos e desenvolvimento de factores de risco cardiovasculares., os factores de risco relevantes para os acontecimentos cardiovasculares associados à domperidona incluem hipertensão, hiperlipidemia, obesidade, diabetes, tabagismo e consumo excessivo de álcool. a domperidona está indicada para sintomas dispépticos associados ao esvaziamento gástrico retardado e sintomas agudos de náuseas e vómitos. não existem dados suficientes que sustentem a utilização de domperidona na doença de refluxo gastro-esofágico infantil e pode não ser adequada para náuseas e vómitos induzidos por quimioterapia ou radioterapia ou para náuseas e vómitos pós – operatórios., outros medicamentos utilizados no tratamento de perturbações digestivas ou náuseas e vómitos também causaram prolongamento do intervalo QTc.discuta com os doentes os benefícios e o risco dos danos do tratamento com domperidona antes de iniciar a terapêutica. Comunicar quaisquer reacções adversas ao centro de monitorização das reacções adversas (CARM).
resumo de revisão
o MARC reviu os últimos dados em junho de 2014. O MARC concluiu que, embora o equilíbrio entre os benefícios e o risco de danos para a domperidona permaneça favorável, existe um pequeno aumento do risco de efeitos cardíacos adversos.,muitos estudos apresentaram um número reduzido de acontecimentos globais e os valores de risco variaram entre os diferentes estudos. Por conseguinte, não foi possível medir uma verdadeira estimativa do risco. Quadro 1: Risco de morte súbita cardíaca: estudo baseado na população de casos de controlo 1.Tabela 2: Risco de arritmia ventricular grave e morte cardíaca súbita com domperidona relativamente à ausência de exposição a medicamentos em estudo ou à exposição a inibidores da bomba de protões: estudo aninhado de caso-controlo da população 2.,
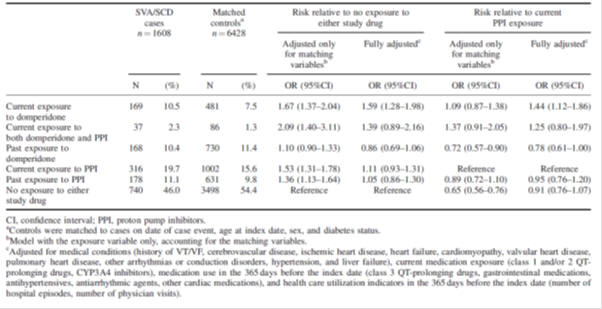
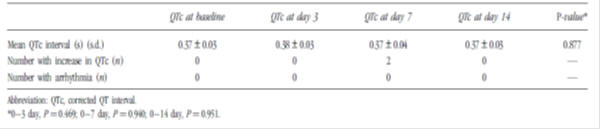
Tabela 3: Avaliação do intervalo QTc antes e durante domperidone administração em prematuros (n=40)3
havia limitações para os estudos incluídos na revisão, tal como a observação da natureza da maioria dos estudos, a falta de informação sobre a indicação para o uso, a gravidade da doença, dose e esquemas, e outros fatores de risco como o tabagismo estado, concomitante de medicamentos e co-morbidades. O viés protopático é quando um tratamento para os primeiros sintomas de uma doença ou outro resultado parece causar o resultado., Nesta situação, os doentes podem ter sido prescritos domperidona para sintomas gastrointestinais não específicos que podem, de facto, ser os sintomas prodromais da doença coronária. Assim, o viés protopático e a confusão por indicação não podem ser excluídos em muitos dos estudos observacionais.os estudos adicionais revistos incluíram um estudo de segurança pós-autorização, bem como estudos que investigaram os efeitos da utilização de domperidona no intervalo QTc em adultos., Um estudo QT completo demonstrou não haver resposta clinicamente relevante dose-QTc ou exposição-QTc com domperidona; contudo, notificações de casos de prolongamento do QTc, arritmia e morte cardíaca súbita com domperidona significam que este risco não pode ser completamente excluído.
O MARC observou que outros tipos de medicamentos utilizados no tratamento de perturbações digestivas ou náuseas e vómitos foram também associados ao prolongamento do intervalo QT. Estes factores devem ser tidos em conta na escolha do melhor medicamento para um doente individual.van Noord C, Dieleman JP, van Herpen G, et al. (2010)., Domperidona e arritmia Ventricular ou morte súbita cardíaca: um estudo de caso de controlo baseado na população nos Países Baixos. Drug Safety, 33 (11): 1003-14
Gunlemez A, Babaoglu A, Arisoy AE, et al. (2010). Efeito da domperidona no intervalo QTc em lactentes prematuros. Journal of Perinatology, 30: 50-3
What actions are Medsafe taking?,a Medsafe está a trabalhar com os patrocinadores destes produtos para assegurar que as fichas de dados e a informação sobre medicamentos para o consumidor delineiem adequadamente a segurança da domperidona.,RAL de aplicativos on-line
Online
Submeter um relatório online
Prescritores pode enviar utilizando o reporting on-line de ferramenta disponível no paciente software de gerenciamento
Cartão Amarelo
Uma concluído cartão Amarelo pode ser enviado para PE via e-mail, fax ou e-mail (o endereço está no cartão)
Email
Fax
(03) 479-7150
Prescritores pode enviar utilizando o reporting on-line de ferramenta disponível no paciente software de gerenciamento
Medsafe não podemos dar conselhos sobre uma pessoa com condição de saúde., Se tem alguma preocupação com um medicamento que está a tomar Medsafe encoraja-o a falar com o seu profissional de saúde.